10月10个品种获批新适应症,12个品种首家过评,这4家企业仿制申报最多
编辑说:2024年10月,4个1类新药、10个改良型新药申报上市;241个品种按新分类仿制申请申报,其中39个品种暂无国内仿制获批,富马酸伏诺拉生片有7家企业提交仿制申请,有4家企业仿制申报品种数最多,各有4个;28个存量品种有企业申报一致性评价,其中1个品种为首次申报;5个1类新药、1个新复方制剂获批上市,10个品种获批新适应症;12个品种首家过评,其中5个为首仿。
来源:米内网原创 2024-11-05 09:56CDE月评菜小白
摘要
2024年10月,4个1类新药、10个改良型新药申报上市;241个品种按新分类仿制申请申报,其中39个品种暂无国内仿制获批,富马酸伏诺拉生片有7家企业提交仿制申请,有4家企业仿制申报品种数最多,各有4个;28个存量品种有企业申报一致性评价,其中1个品种为首次申报;5个1类新药、1个新复方制剂获批上市,10个品种获批新适应症;12个品种首家过评,其中5个为首仿。
创新药品种申报情况
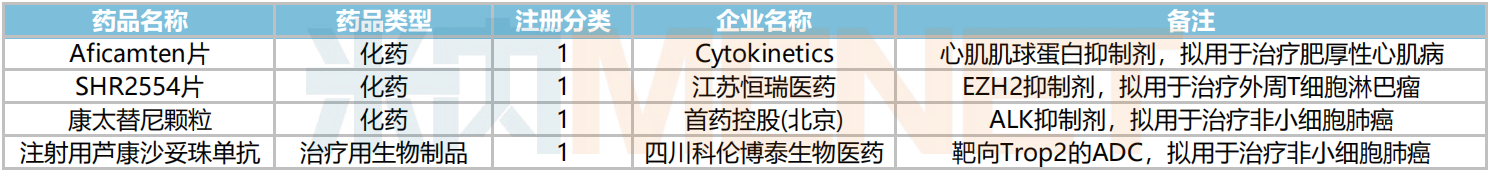
2024年10月,133个创新药品种(药品注册分类为“1”的品种)获CDE承办。4个品种申请上市:Aficamten片(Cytokinetics)、SHR2554片(江苏恒瑞医药)、康太替尼颗粒(首药控股(北京))、注射用芦康沙妥珠单抗(四川科伦博泰生物医药)。
2024年10月创新药上市申请承办情况
2024年10月创新药临床申请承办情况


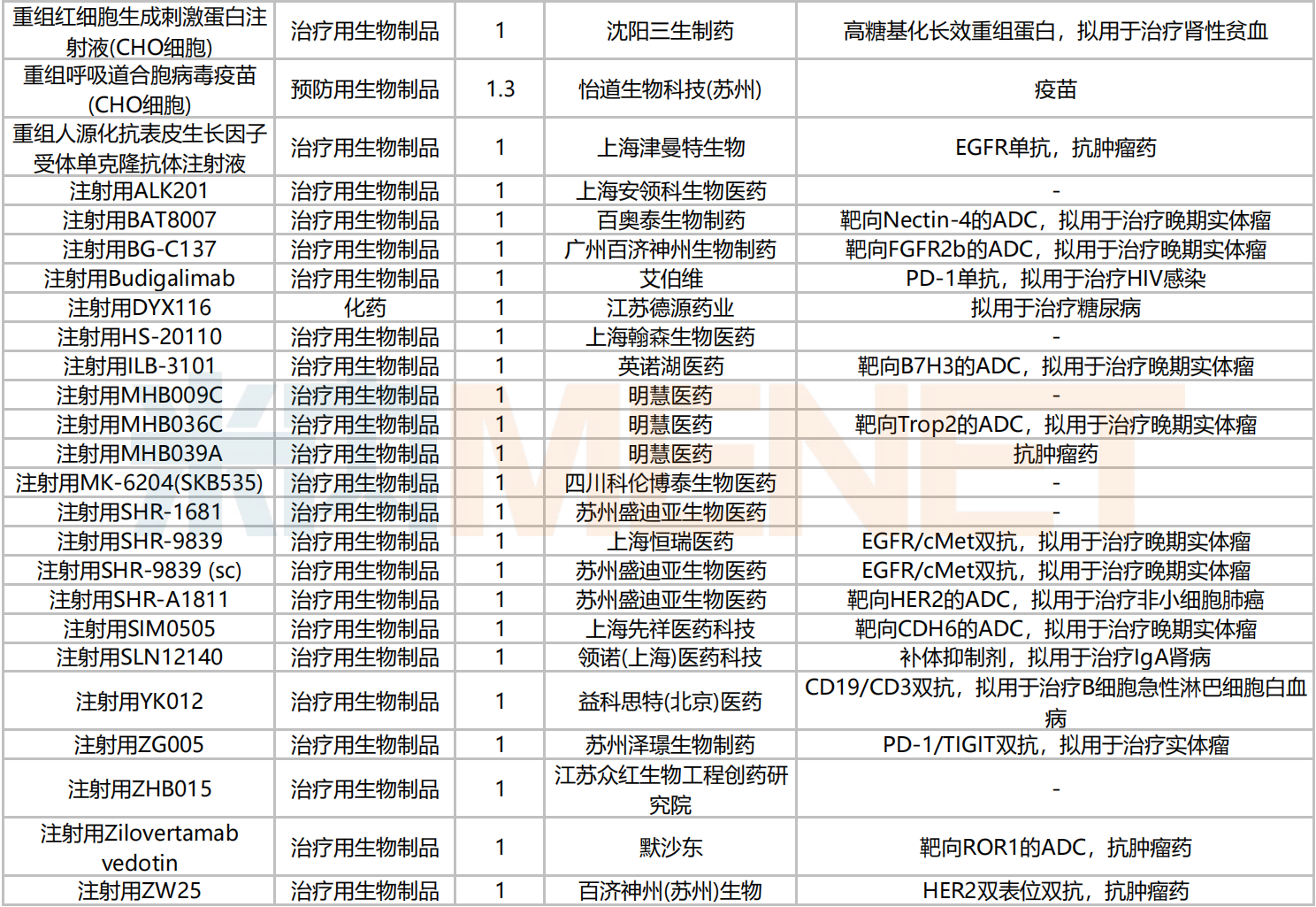
改良型新药品种申报情况
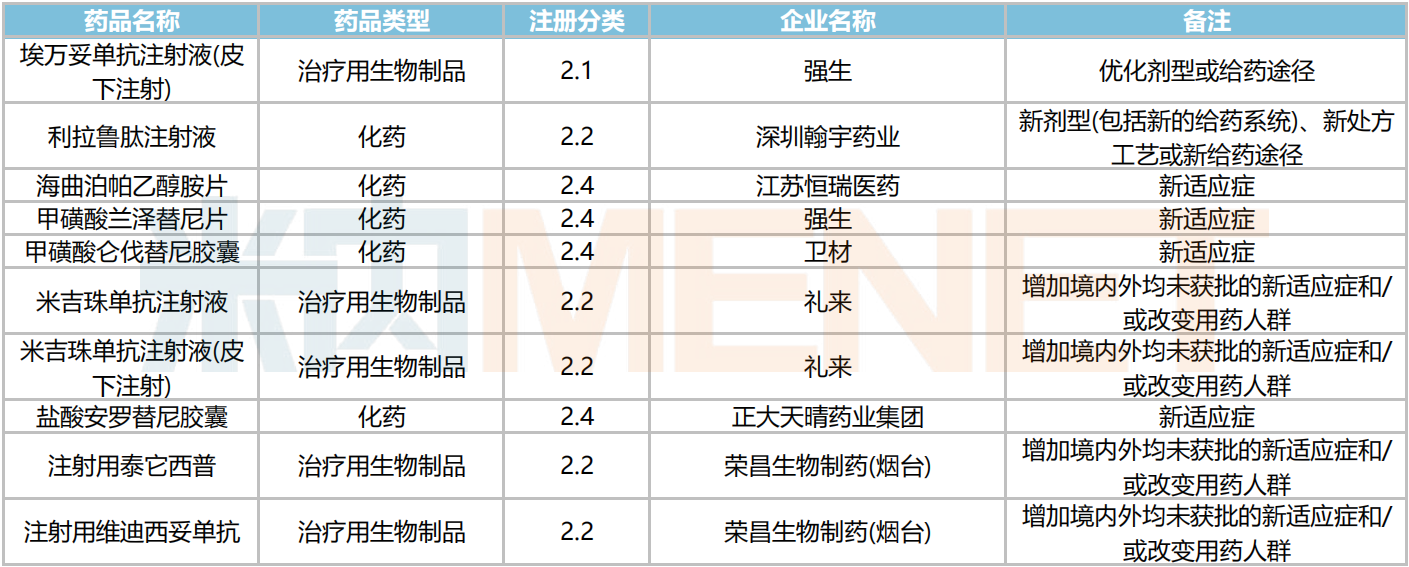
2024年10月,50个改良型新药品种获CDE承办。埃万妥单抗注射液(皮下注射)(强生)以及利拉鲁肽注射液(深圳翰宇药业)为剂型优化或新给药途径,海曲泊帕乙醇胺片(江苏恒瑞医药)、甲磺酸兰泽替尼片(强生)、甲磺酸仑伐替尼胶囊(卫材)、米吉珠单抗注射液(礼来)、米吉珠单抗注射液(皮下注射)(礼来)、盐酸安罗替尼胶囊(正大天晴药业集团)、注射用泰它西普(荣昌生物制药(烟台))、注射用维迪西妥单抗(荣昌生物制药(烟台))8个品种为新适应症上市申请。
2024年10月改良型新药上市申请承办情况
2024年10月改良型新药临床申请承办情况
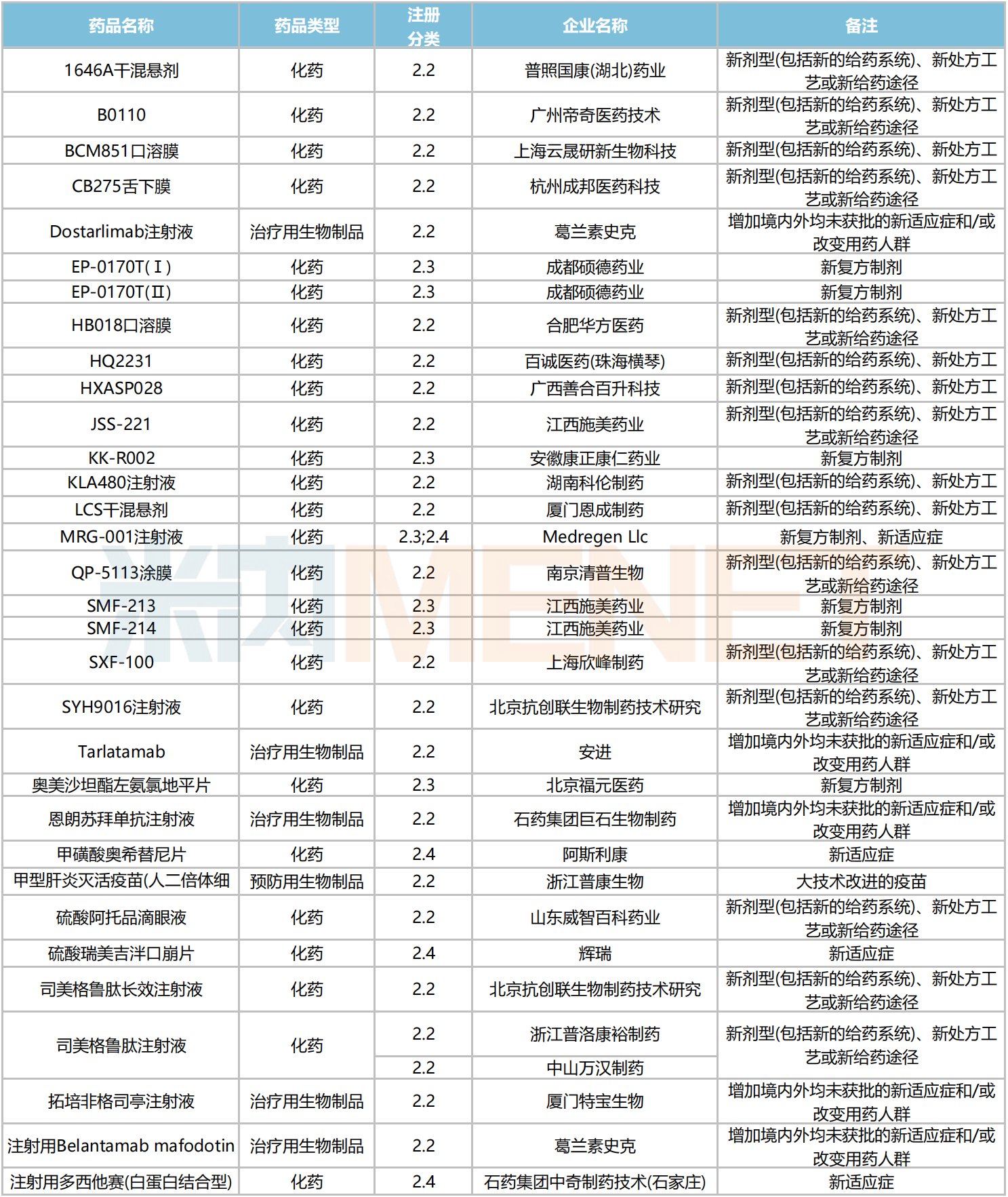
新分类仿制药品种申报情况
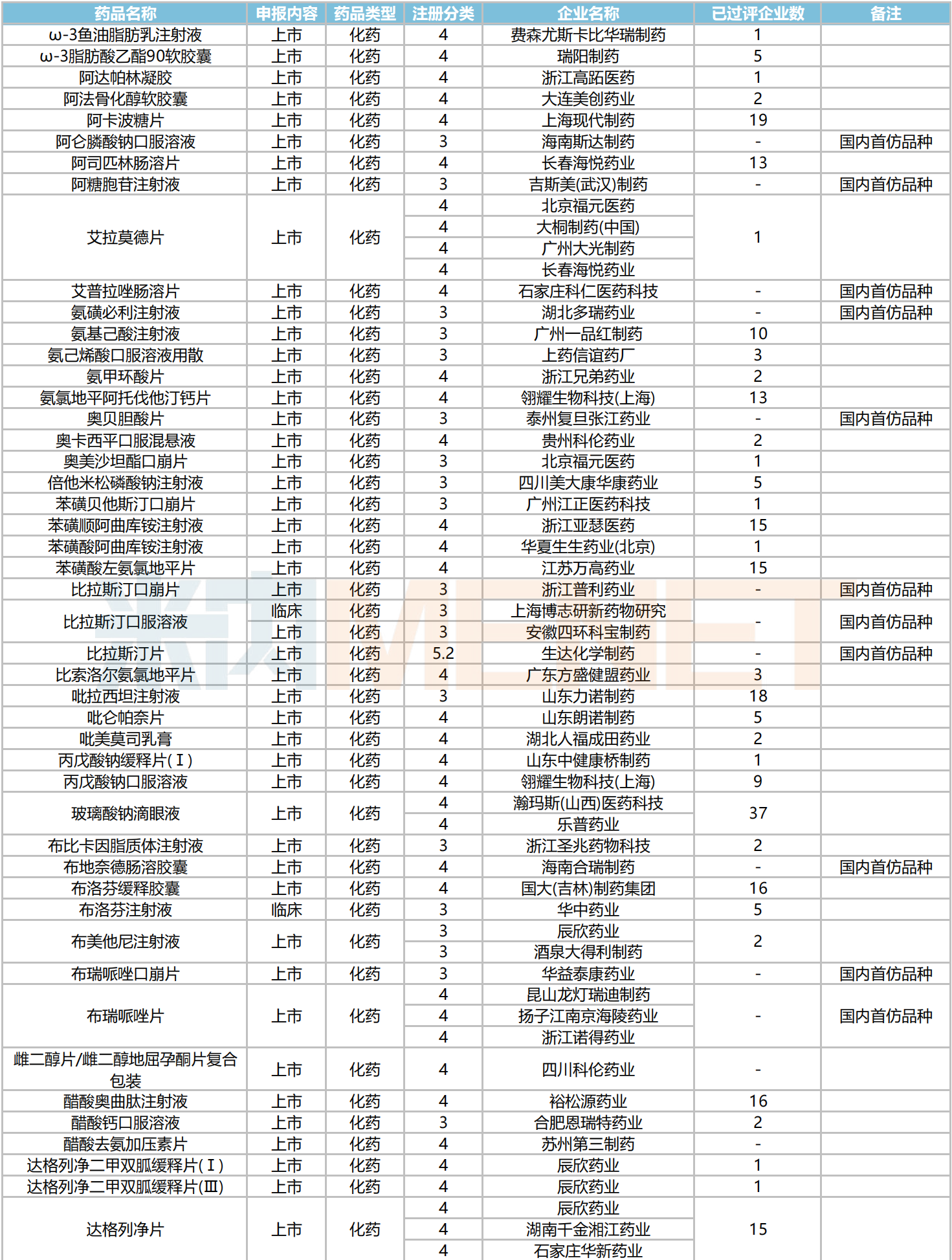
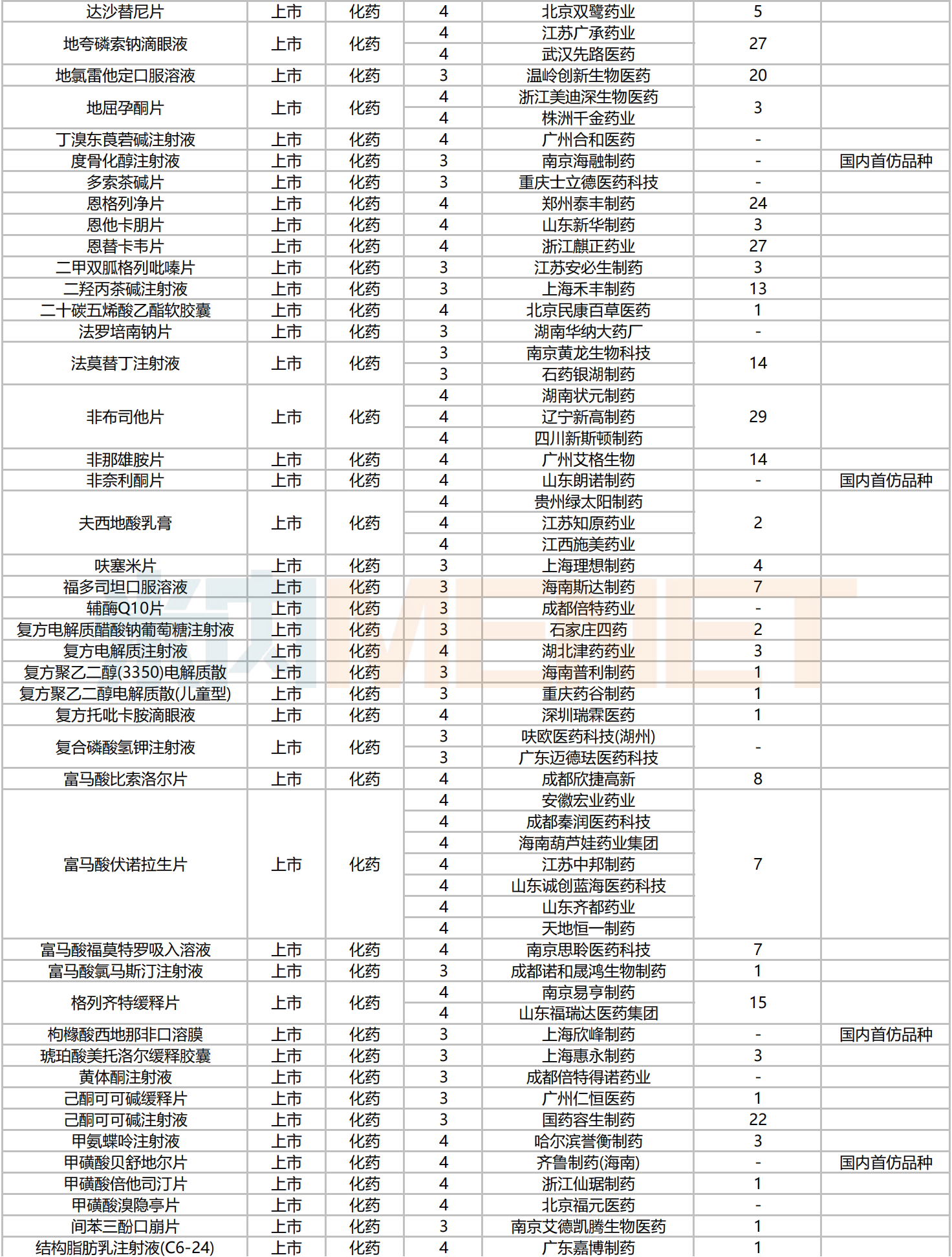
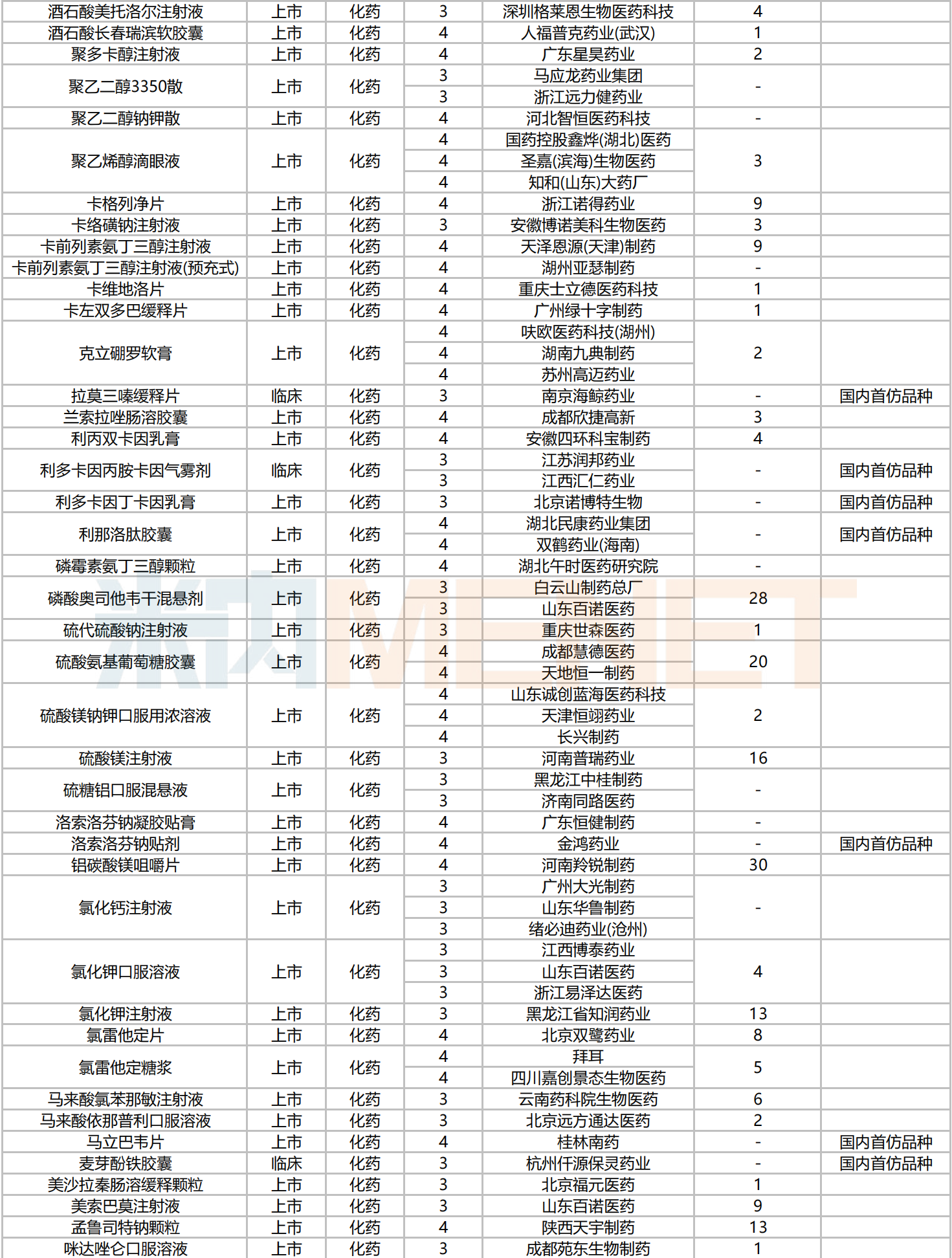
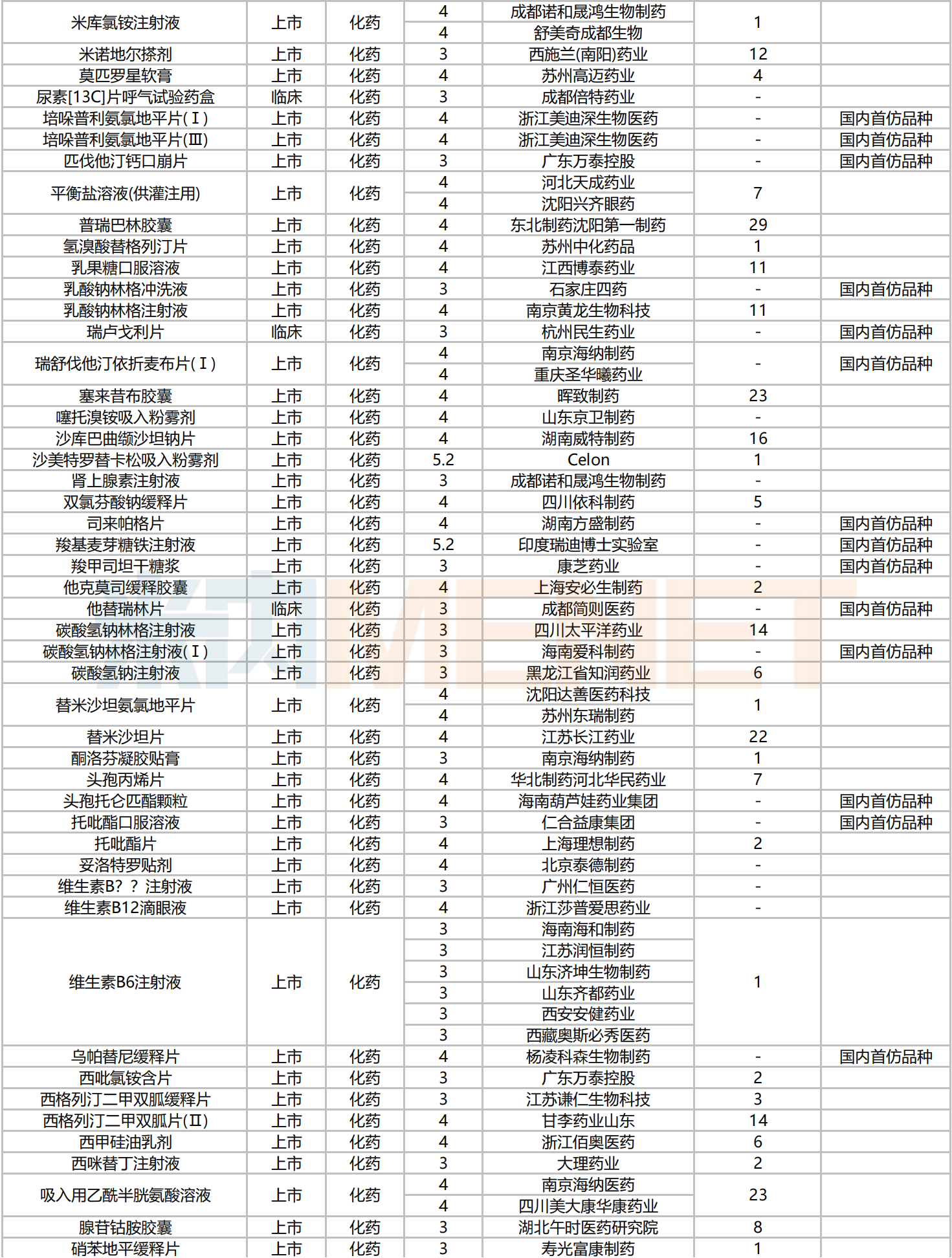
2024年10月,241个品种仿制申请获CDE承办,其中39个品种目前暂无国内仿制药获批。富马酸伏诺拉生片的仿制申请企业最多,有7家:安徽宏业药业、成都秦润医药科技、海南葫芦娃药业集团、江苏中邦制药、山东诚创蓝海医药科技、山东齐都药业、天地恒一制药。此外,山东齐都药业、山东百诺医药、辰欣药业、北京福元医药等企业的申报品种数最多,均有4个。
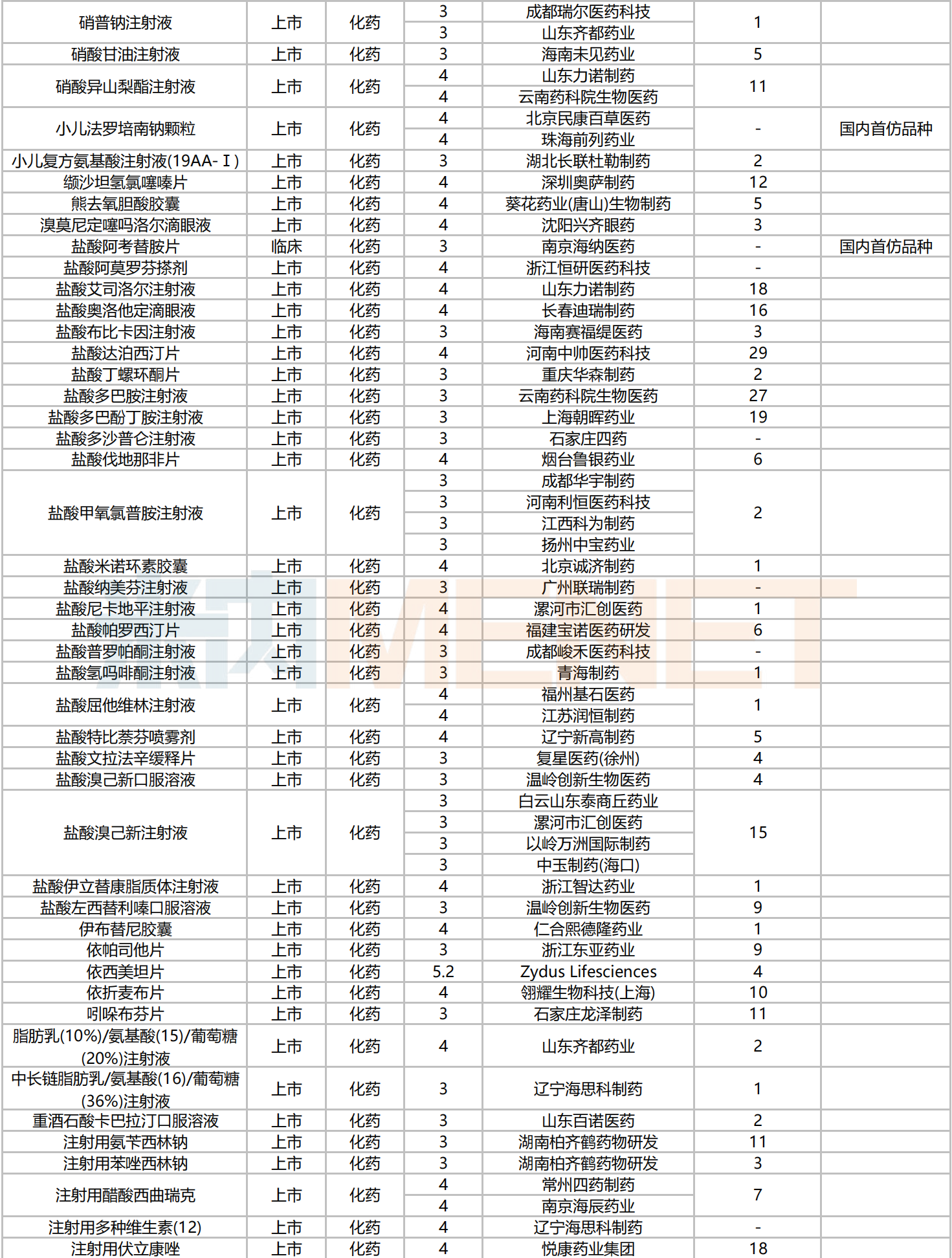
2024年10月新分类仿制药品种申报情况
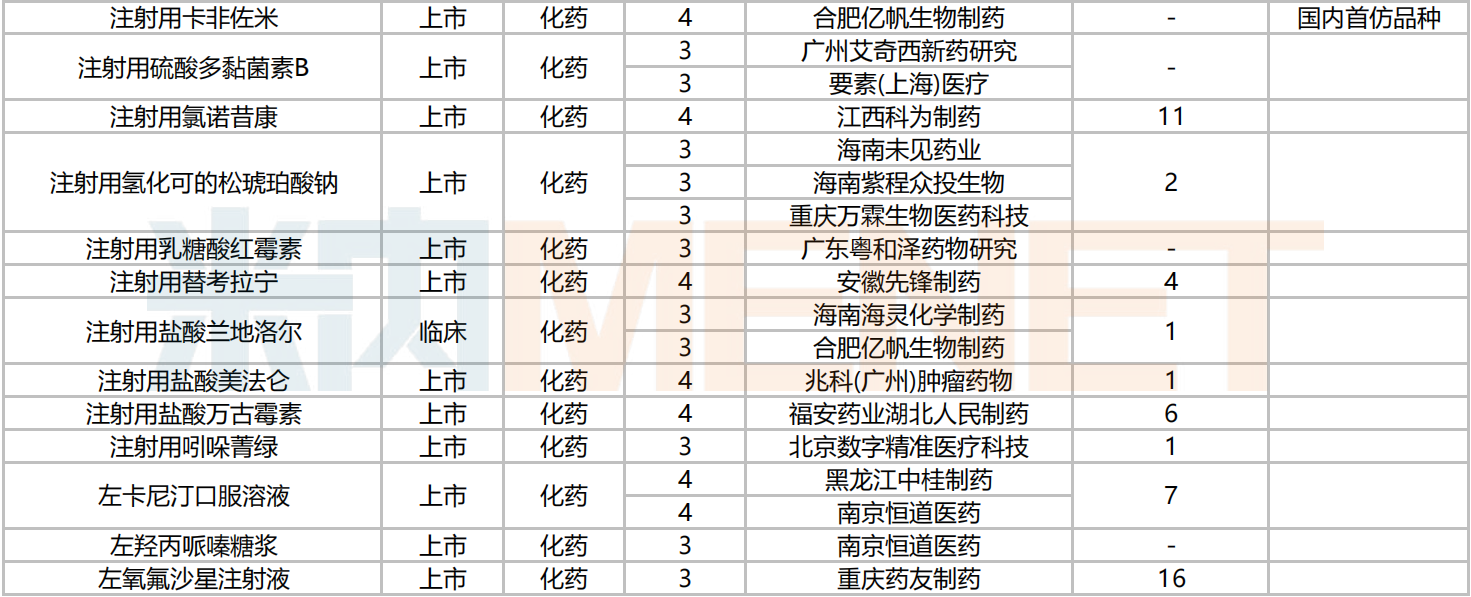
存量品种一致性评价申报情况
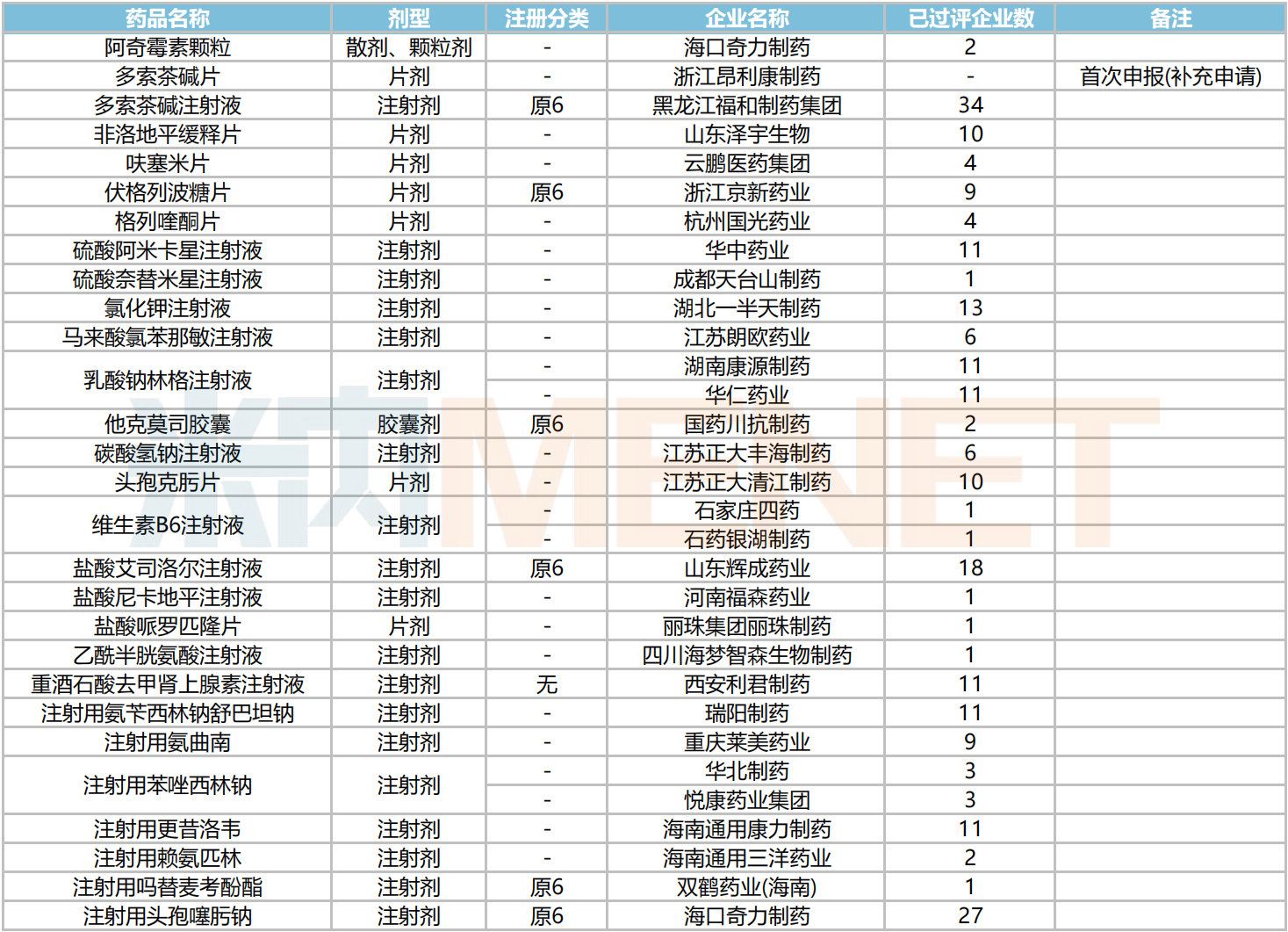
2024年10月,28个品种的一致性评价补充申请获CDE承办。多索茶碱片首次有企业按补充申请申报。
2024年10月存量品种一致性评价申报情况
获批情况
2024年10月有5款1类新药首次获批上市:艾帕洛利托沃瑞利单抗注射液(齐鲁制药)、昂戈瑞西单抗注射液(上海君实生物医药科技)、夫那奇珠单抗注射液(苏州盛迪亚生物医药)、甲磺酸普雷福韦片(西安葛蓝新通制药)、伊努西单抗注射液(康融东方(广东)医药),尼拉帕利阿比特龙片(强生)为新复方制剂。此外,还有10个品种获批新适应症。
139个品种按新分类仿制申请获批并视同过评,54个品种按存量品种一致性评价补充申请过评。有12个品种首家过评,其中,波生坦片(北京四环科宝制药)、复方聚乙二醇(3350)电解质维C散(舒泰神(北京)生物制药)、来特莫韦注射液(南京正大天晴制药)、利奥西呱片(齐鲁制药)、美沙拉秦肠溶缓释颗粒(江苏安必生制药)5个品种为国内首仿。
2024年10月主要注册类型品种获批情况
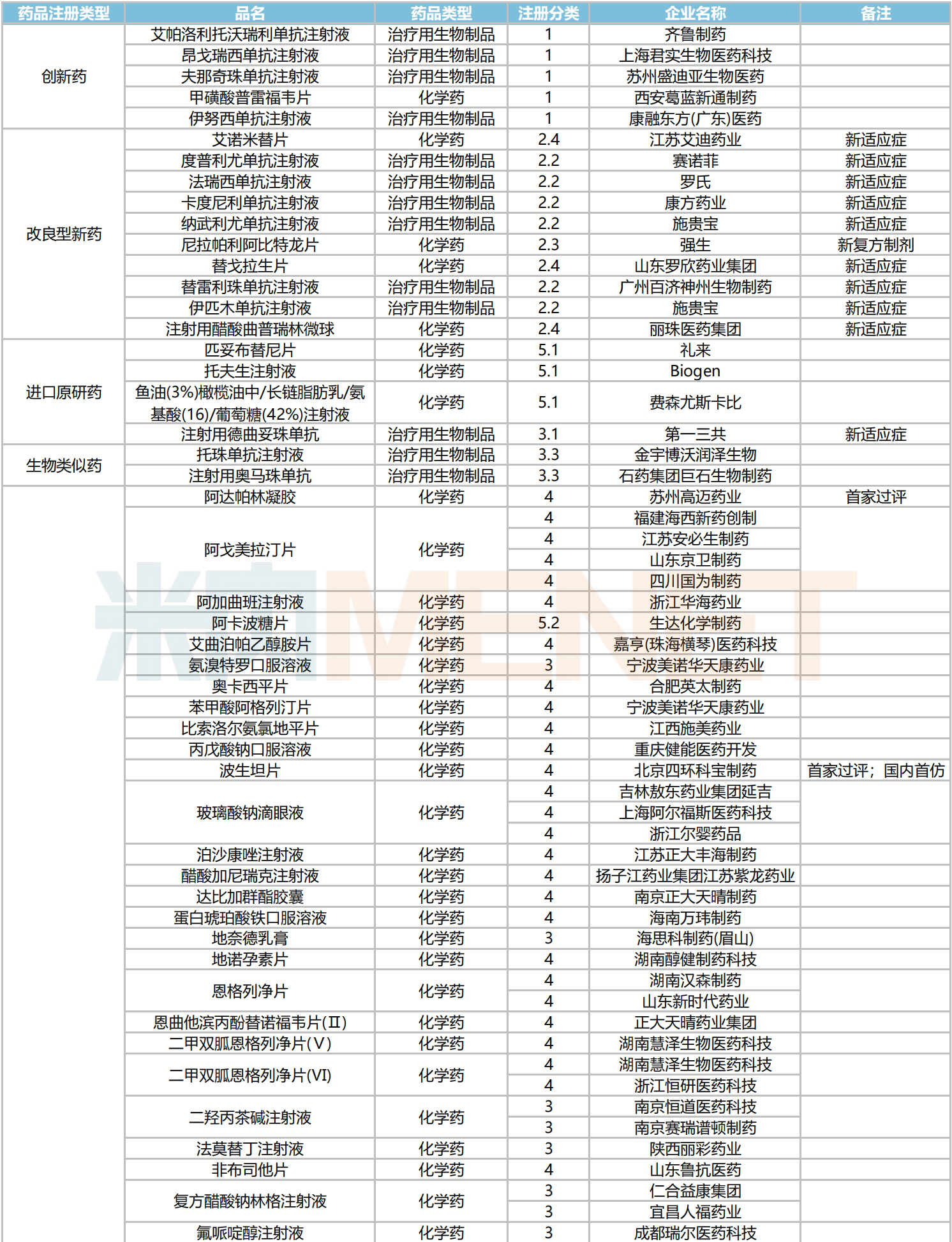
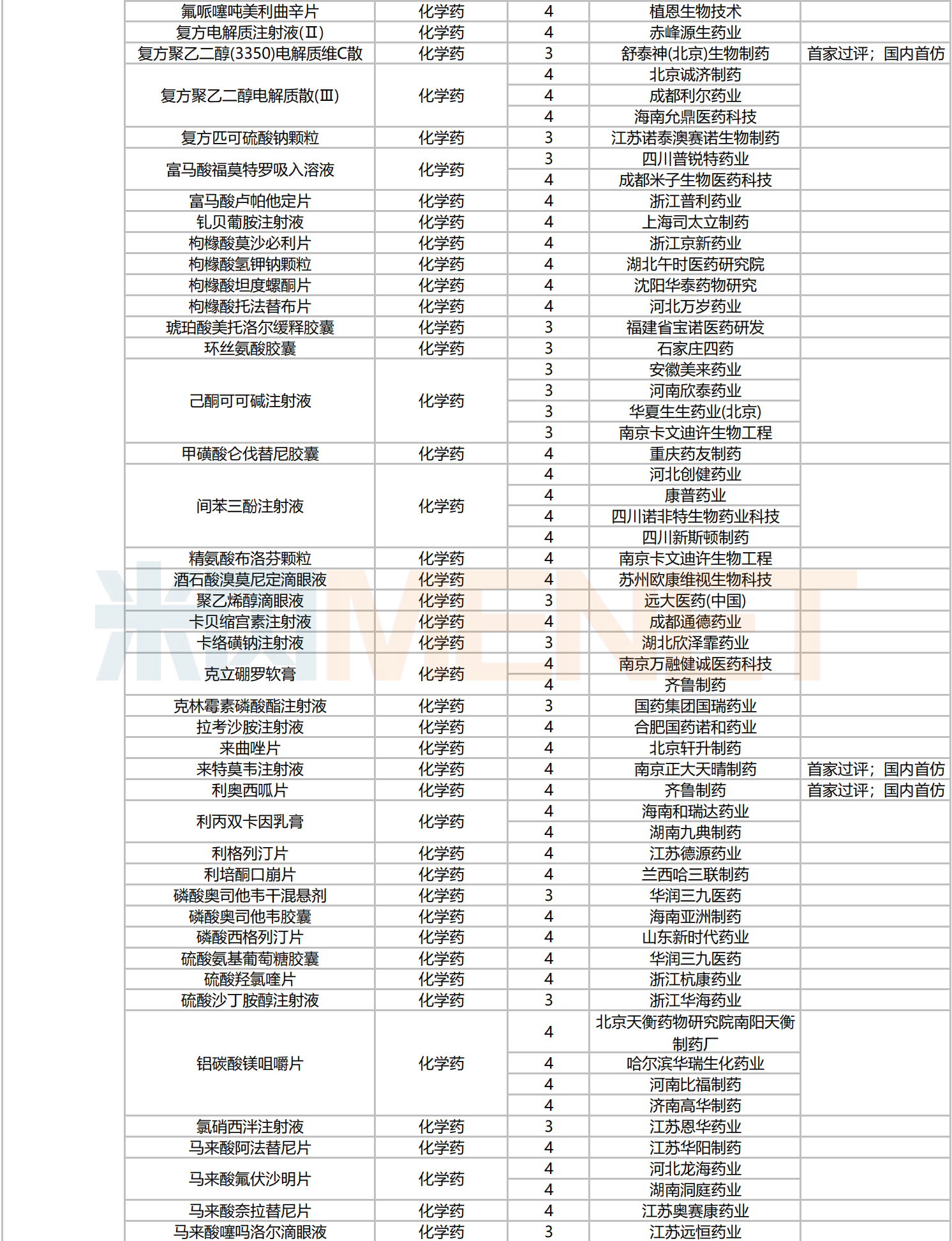
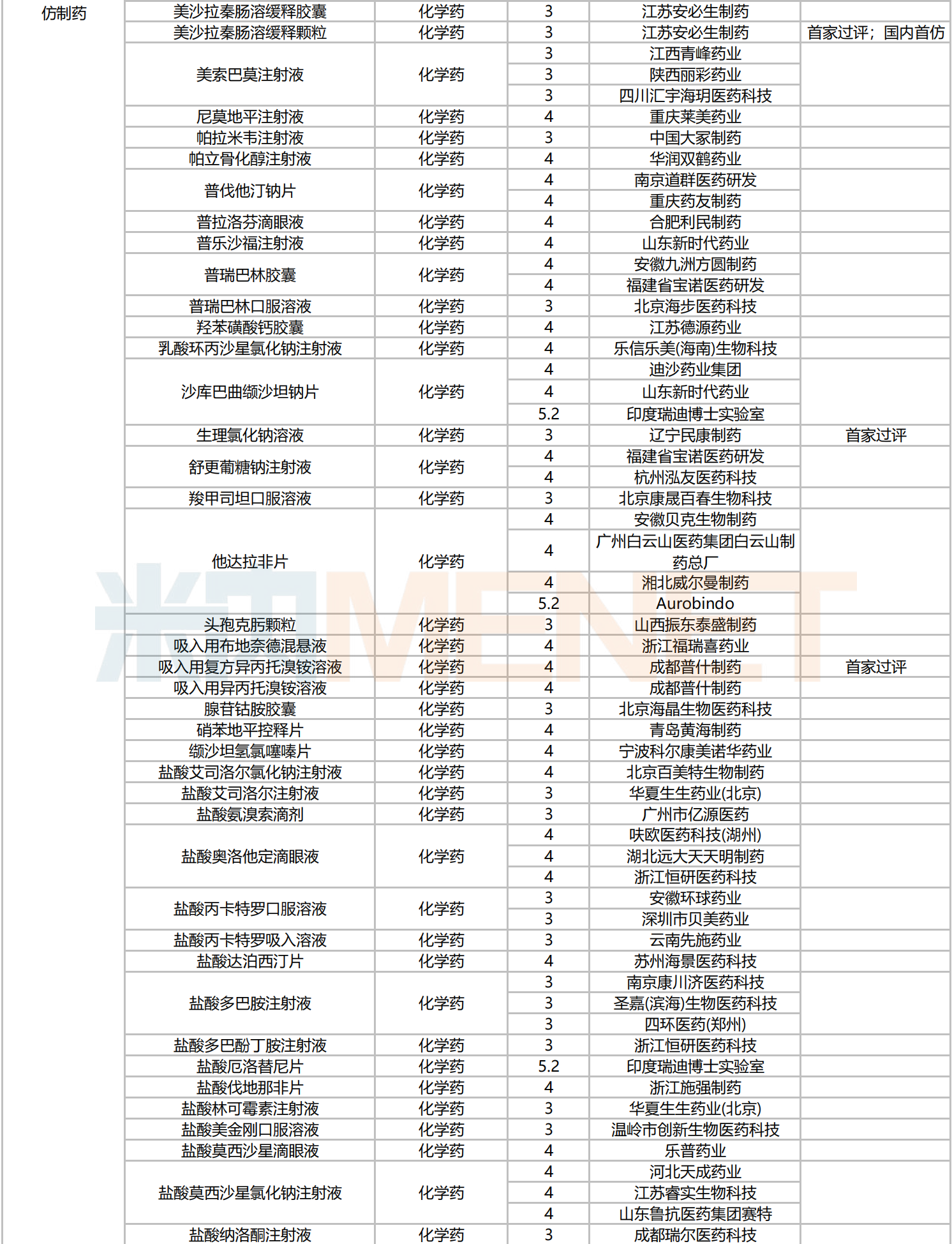

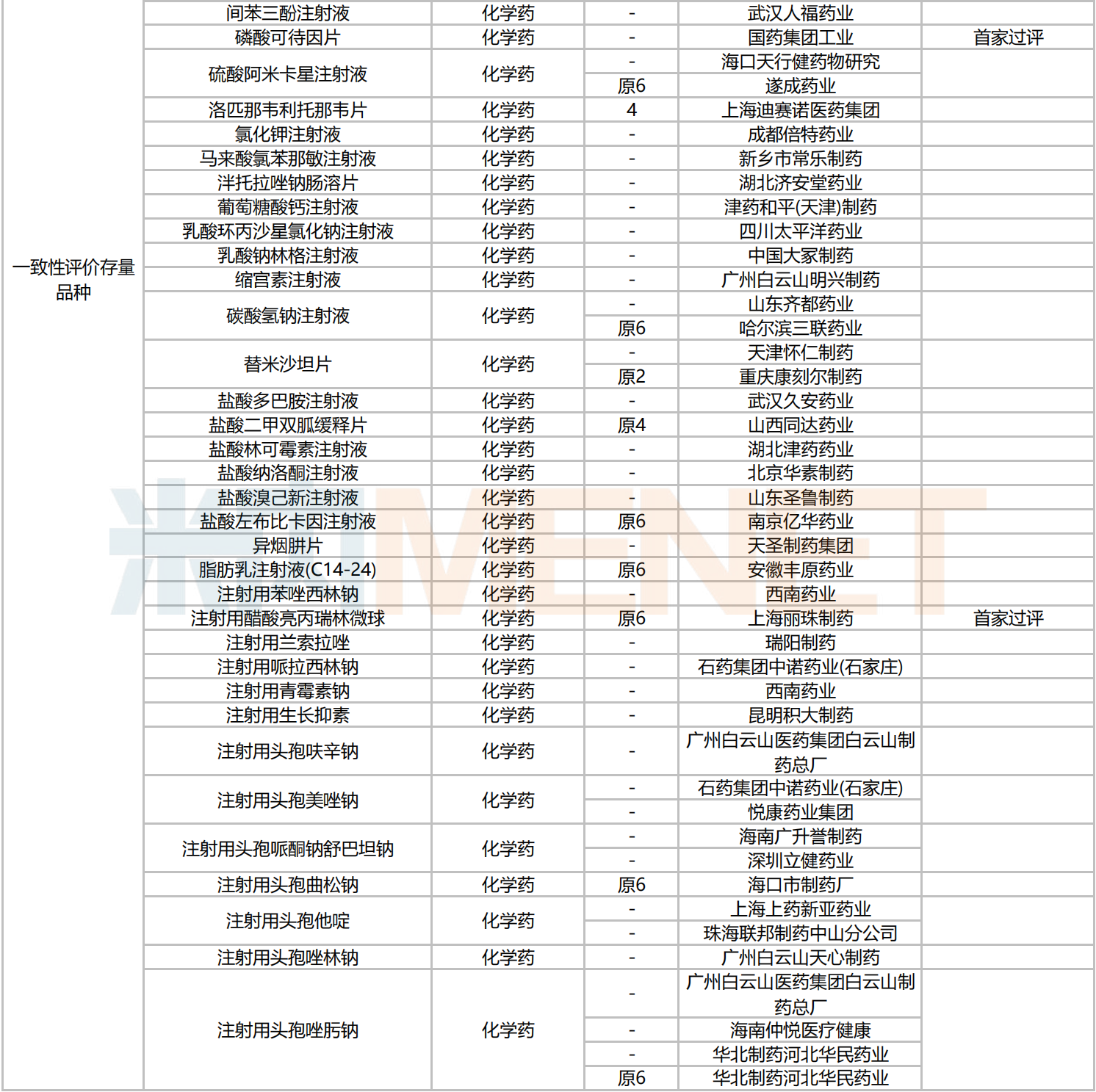
数据来源:米内网中国申报进度数据库(MED)、CDE、NMPA;相关统计字段按药品名称统计,申报企业数按主申报企业统计,时间截至2024年10月31日;获批品种按NMPA发布时间统计;药物作用靶点以及适应症整理自公开资料。



